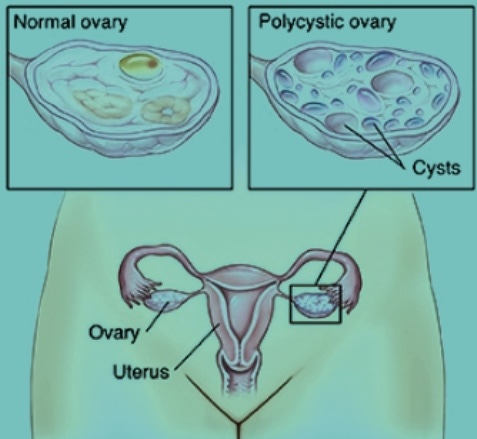
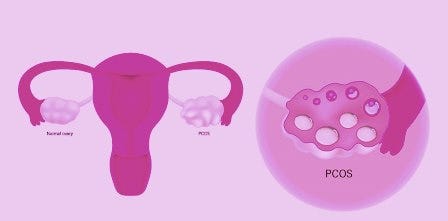
O estrogênio na síndrome do ovário policístico [PCOS]
O estrogênio transcende, de longe, seu rótulo de “hormônio feminino”
[Imagem: saintlukeskc.org]
A experiência foi publicada em 1993, no jornal Endocrinology [A], mas aparentemente as coisas funcionam como se ela não tivesse existido: congressos médicos e os próprios protocolos relacionados ao problema da síndrome do ovário policístico [PCOS em inglês] continuam como antes, isto é, não levaram em conta a cabal demonstração daquela experiência com ratas.
Como foi a experiência.
Injetaram estrogênio [valerato de estradiol][D] em fêmeas e o resultado foi o aparecimento de ovário policístico. Zero dúvida: estrogênio em excesso promove PCOS.
No mesmo experimento, também ficou claro que o excesso de estrogênio ativou o eixo hipófise-adrenal, por exemplo, com ativação dos neurônios periféricos do simpático que inervam o ovário, que passaram a liberar adrenalina, com aumento do teor de nor-epinefrina nos ovários. Provavelmente tendo a ver com efeitos do tipo androgenização que aparecem em PCOS.
Depois disso, também vierem evidências, a cada década, da associação, agora em mulheres, entre dominância estrogênica e ovário policístico.
Não somente PCOS mas também outros problemas do aparelho reprodutor feminino e câncer. Aliás, não resta dúvida que o estrogênio – longe de operar como apenas um “hormônio feminino” age em todos os sistemas do organismo, começando pela respiração celular oxidativa e pela regulação da água na célula [aumentando sua retenção].
Por outro lado, basta que a pessoa desenvolva um processo de hipotireoidismo para que o organismo passe a fabricar abundantemente o estrogênio. Também a adrenalina. Essa relação foi demonstrada sucessivas vezes e R. Peat é pioneiro em chamar a atenção sobre essa relação e o holismo entre os hormônios.
O impacto do excesso de estrogênio sem oposição da progesterona no corpo será sistêmico, embora desigual e combinado, isto é, atingindo alguns órgãos e funções antes que outros. Para se ter graves problemas, basta que o organismo não sintetize suficiente progesterona para fazer oposição ao estrogênio.
Mas será sistêmico o efeito.
Como já argumentou R. Peat “o estrogênio, ao menos quando não encontra oposição por parte de uma grande concentração de progesterona, cria todas as condições conhecidas que estão envolvidas no processo de envelhecimento.
Tais efeitos do estrogênio incluem interferência com o metabolismo oxidativo, formação de lipofucsina [o prigmento da idade], retenção de ferro, produção de radicais livres e peroxidaçao lipídica, promoção de excitotoxicidade e morte de células nervosas, comprometimento da capacidade de aprendizado, aumentada tendência a formar coágulos sanguíneos e de apresentar espasmos vasculares, aumentada autoimunidade e atrofia do timo; elevada prolactina, atrofia da pele, aumentada susceptibilidade a uma grande variedade de cânceres, temperatura corporal diminuída, queda na albumina sérica, aumentada tendência a edema e muitas das características do choque.
Em anos recentes foi descoberta a responsabilidade do estrogênio mesmo em masculinização do bebê e no processo de masculinização que integra a síndrome do ovário policístico. Embora a indústria farmacêutica sempre se referiu ao estrogênio como o ´hormônio feminino´, não conheço nenhum cientista competente que se anime a chamá-lo assim”.
[Imagem: draliabadi.com]
Esse mesmo autor acrescenta que “além de trazer novos insights em relação a processos como energia biológica e envelhecimento, o reconhecimento de que o estrogênio ativa o sistema de hormônios do estresse, sistema hipófise-adrenal, também traz claros insights em relação a outros problemas, como a síndrome do ovário policístico, o hirsutismo [excesso de pelos], hiperplasia da adrenal e doença de Cushing dentre outros“ [R. Peat].
Há trabalhos mostrando que PCOS é uma doença ovariana que vem acompanhada de hipeestrogenização e hiperandrogenização e “todos os estudos mostraram que hiperestrogenemia é o resultado de uma elevação da estrona e estradiol no plasma” [B].
Enquanto isso está em escalada o aparecimento de PCOS em adolescentes. “Irregularidades menstruais e sinais cutâneos de excesso de andrógenos são comumente encontradas em adolescentes. PCOS é a mais frequente causa de tais sintomas em mulheres adultas e também em adolescentes” [F].
O trabalho acima citado [B] menciona que encontraram um caso de ovário policístico no qual “o estradiol plasmático estava tão elevado que mimetizava a produção de estrogênio do nível de um câncer” [B].
Sim, vários tipos de câncer produzem estrogênio massivamente [embora nenhum produza progesterona é sempre importante observar].
No PCOS, a massiva presença de estrogênio é que induziria uma sensibilidade ovariana e hipofisária [ACTH] alterando, também, a produção de andrógenos [C].
Qual a primeira ironia nisso tudo? Ginecologistas continuam prescrevendo, para o ovário policístico, a pílula de ... estrogênio.
A outra ironia: uma vez sabido que é possível – demonstrado há décadas – que podemos criar síndrome do ovário policístico em animais fêmeas, com simples injeções de estrogênio, por que os congressos médicos simplesmente não se ocupam de decifrar esse problema focando na relação estrogênio-PCOS na mulher? Ou focando na relação mais básica tireoide-estrogênio-progesteronaɁ
Em 2009, ainda continuavam produzindo PCOS em ratas com injeção de estrogênio [E]. Quousque tandemɁ
Talvez uma questão para ser conversada pacientemente com o seu ginecologista mais próximo.
GM Fontes, Brasília, 7-5-23
As informações aqui presentes não pretendem servir para uso diagnóstico, prescrição médica, tratamento, prevenção ou mitigação de qualquer doença humana. Não pretendem substituir a consulta ao profissional médico ou servir como recomendação para qualquer plano de tratamento. Trata-se de informações com fins estritamente educativos.
Referências ________________
[A] BARRIA A, LEYTON V, 1993. Ovarian steroidal response to gonadotropins and beta-adrenergic stimulation is enhanced in polycystic ovary syndrome: role of sympathetic innervation. Endocrinology . 1993 Dec;133(6):2696-703. doi: 10.1210/endo.133.6.8243293. PMID: 8243293 DOI: 10.1210/endo.133.6.8243293 “Experimental induction of a polycystic ovarian syndrome (PCOS) in rodents by the administration of a single dose of estradiol valerate (EV) results in activation of the peripheral sympathetic neurons that innervate the ovary. This activation is evidenced by an increased capacity of ovarian nerve terminals to incorporate and release norepinephrine (NE), an increase in ovarian NE content, and a decrease in ovarian beta-adrenergic receptor number in the ovarian compartments receiving catecholaminergic innervation. The present experiments were undertaken to examine the functional consequences of this enhanced sympathetic outflow to the ovary. The steroidal responses of the gland to beta-adrenergic receptor stimulation and hCG were examined in vitro 60 days after EV administration, i.e. at the time when follicular cysts are well established. EV-treated rats exhibited a remarkable increase in ovarian progesterone and androgen responses to isoproterenol, a beta-adrenergic receptor agonist, with no changes in estradiol responsiveness. Basal estradiol release was, however, 50-fold higher than the highest levels released from normal ovaries at any phase of the estrous cycle. The ovarian progesterone and androgen responses to hCG were enhanced in EV-treated rats, as were the responses to a combination of isoproterenol and hCG. Transection of the superior ovarian nerve (SON), which carries most of the catecholaminergic fibers innervating endocrine ovarian cells, dramatically reduced the exaggerated responses of all three steroids to both beta-adrenergic and gonadotropin stimulation. SON transection also reduced the elevated levels of ovarian NE resulting from EV treatment and caused up-regulation of beta-adrenoreceptors. Most importantly, SON transection restored estrous cyclicity and ovulatory capacity. The results indicate that the increased output of ovarian steroids in PCOS is at least in part due to an enhanced responsiveness of the gland to both catecholaminergic and gonadotropin stimulation. The ability of SON transection to restore a normal response indicates that the alteration in steroid output results from a deranged activation of selective components of the noradrenergic innervation to the ovary. These findings support the concept that an alteration in the neurogenic control of the ovary contributes to the etiology of PCOS”.
[B] BENJAMIN, F, TOLES A W, 1993. Excessive estradiol secretion in polycystic ovarian disease. Am J Obstet Gynecol. 1993 Nov;169(5):1223-6. doi: 10.1016/0002-9378(93)90286-r. PMID: 8238188 DOI: 10.1016/0002-9378(93)90286-r “Polycystic ovarian disease is both a hyperestrogenic and a hyperandrogenic syndrome, and all studies have shown that hyperestrogenemia is the result of an elevation of estrone with plasma estradiol levels in the normal follicular range. Because a literature search failed to reveal any report of polycystic ovarian disease with significantly elevated estradiol levels, we report a case in which the plasma estradiol was so massively elevated as to mimic an estrogen-producing neoplasm. This case also suggests that although polycystic ovarian disease is a very rare cause of such excessive estradiol production, it should be included in the differential diagnosis of estrogen-producing neoplasms”.
[C] DITKOFF E C FRUZZETTI< F, 1995. The impact of estrogen on adrenal androgen sensitivity and secretion in polycystic ovary syndrome. J Clin Endocrinol Metabolismo. 1995 Feb;80(2):603-7. doi: 10.1210/jcem.80.2.7852527. PMID: 7852527 DOI: 10.1210/jcem.80.2.7852527 “Adrenal hyperandrogenism is a common feature of patients with polycystic ovary syndrome (PCO). This may be due to enhanced adrenal sensitivity to ACTH. Because enhanced ovarian androgen secretion does not appear to explain this phenomenon, we explored the role of estrogen in inducing enhanced adrenal sensitivity, in that a state of relative hyperestrogenism exists in PCO. Eight patients with PCO and seven matched controls received ovine corticotropin-releasing hormone (oCRH; 0.1 micrograms/kg) iv before and after hypoestrogenism was induced by leuprolide acetate (LA; 1 mg, sc, each day). In patients with PCO, a third oCRH test was repeated after transdermal estradiol (E2; 0.1 mg) had been applied for a week, during which time LA was continued. At baseline, patients with PCO had increased responses of 11 beta-hydroxyandrostenedione and dehydroepiandrosterone (P < 0.03 and P < 0.02) and increased delta maximal ratios of androstenedione (A4)/ACTH and dehydroepiandrosterone/ACTH (P < 0.01) after oCRH treatment. After LA administration to patients with PCO, these ratios were significantly suppressed (P < 0.01) and returned to baseline after E2 was added. There were no changes in controls. Steroid ratio responses to oCRH suggested that 17,20-desmolase activity (delta maximum change in the ratio of A4/17-hydroxyprogesterone) was lowered with estrogen suppression and increased again after transdermal E2 administration. There was a significant positive correlation between changes in E2 levels and delta maximum change in the ratios of A4/17-OHP after oCRH treatment, signifying 17,20-desmolase activity (r = 0.58, P < 0.02). In conclusion, these data provide evidence that estrogen is at least one factor that influences adrenal androgen sensitivity in PCO and may help explain the frequent finding of adrenal hyperandrogenism in this syndrome.
[D] Valerato de estradiol é um estrógeno vendido nas farmácias como medicamento portador de estrogênio, como contraceptivo.
[E] CHAPMAN, J C, MIN S H, 2009. The estrogen-injected female mouse: new insight into the etiology of PCOS. Reprod Biol Endocrinol. 2009 May 18;7:47. doi: 10.1186/1477-7827-7-47. PMID: 19450261 PMCID: PMC2695461 DOI: 10.1186/1477-7827-7-47 “Female mice and rats injected with estrogen perinatally become anovulatory and develop follicular cysts. [,,,] We propose that in utero exposure to excessive levels of steroids such as estrogen has a long-term effect on the ability of the thymus to produce regulatory T cells. In female offspring this can lead to PCOS”.
[F] DiVALL, S, MERJANEH, L, 2019. Adolescent Polycystic Ovary Syndrome: An Update. Pediatr Ann . 2019 Aug 1;48(8):e304-e310. doi: 10.3928/19382359-20190729-01. PMID: 31426098 DOI: 10.3928/19382359-20190729-01 “Menstrual irregularities and cutaneous signs of androgen excess are commonly encountered when caring for adolescent girls. Polycystic ovary syndrome (PCOS) is the most common cause of these symptoms in adult women, and it can be diagnosed in adolescents as well”. [Pediatr Ann. 2019;48(8):e304-e310.].
***